La grossesse constitue l’un des déclencheurs hormonaux les plus puissants dans l’histoire naturelle du lipœdème. Les bouleversements endocriniens qui accompagnent la gestation — hyperstrogénie gestationnelle, imprégnation progestative, résistance physiologique à l’insuline, activation du système rénine-angiotensine-aldostérone — créent un terrain métabolique et vasculaire propice à l’apparition ou à l’aggravation d’un lipœdème. Cet article expose les mécanismes hormonaux en jeu durant la grossesse et le post-partum, décrit les manifestations cliniques spécifiques à cette période et présente les options thérapeutiques disponibles, notamment la prise en charge chirurgicale spécialisée disponible en Tunisie.
Introduction
La grossesse représente une période de profonde transformation hormonale qui, chez les femmes génétiquement prédisposées, peut précipiter l’apparition d’un lipœdème ou aggraver significativement une maladie préexistante. Alors que de nombreuses femmes attribuent à tort la prise de poids et les modifications corporelles de la grossesse à une simple surcharge pondérale, un sous-groupe important développe en réalité une redistribution pathologique du tissu adipeux caractéristique du lipœdème [1].
L’enjeu diagnostique est considérable : une grossesse peut ainsi constituer la première manifestation clinique révélatrice d’un lipœdème, ou transformer un stade I asymptomatique en stade II ou III invalidant. La compréhension des mécanismes hormonaux en jeu est indispensable pour permettre un diagnostic précoce, adapter la prise en charge pendant et après la grossesse, et éviter les erreurs thérapeutiques — notamment les régimes restrictifs inadaptés ou les tentatives de drainage insuffisamment spécialisées.
La prévalence du lipœdème parmi les femmes en âge de procréer est estimée entre 10 et 18 %, mais sa reconnaissance au décours d’une grossesse reste exceptionnellement rare dans la pratique courante, faute de formation spécifique des équipes obstétricales et de médecine générale [2].
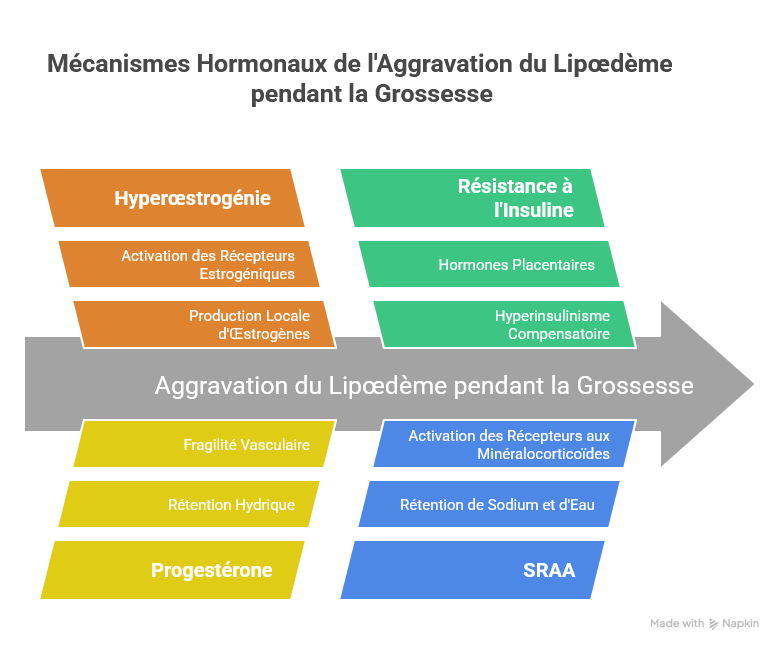
Mécanismes hormonaux de la grossesse et lipœdème
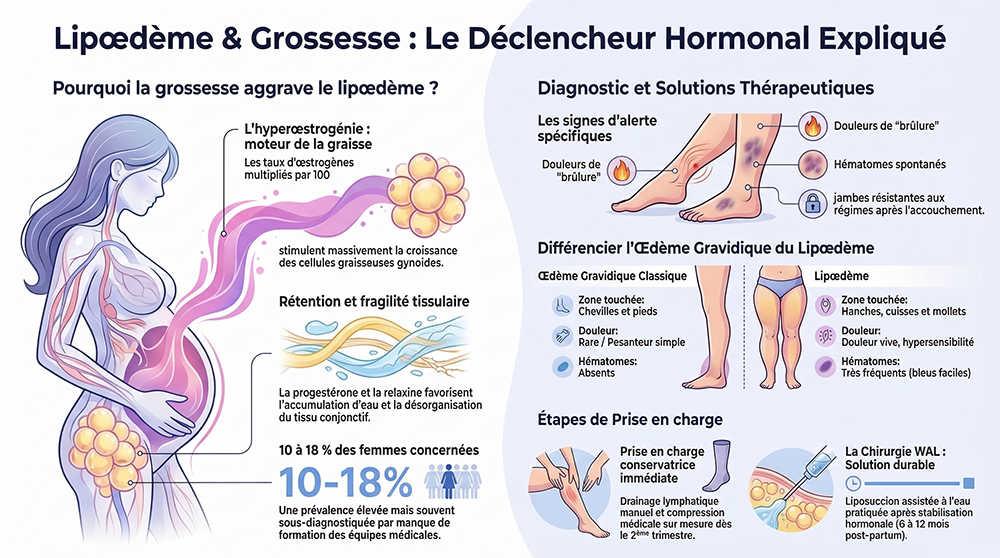
L’hyperstrogénie gestationnelle : moteur de la lipogenèse localisée
Dès les premières semaines de grossesse, les taux d’œstradiol s’élèvent de façon exponentielle, multipliés par 100 à 1 000 par rapport aux valeurs basales du cycle menstruel. Ces concentrations massives d’œstrogènes activent puissamment les récepteurs estrogéniques ER-α présents dans les préadipocytes des régions gynoïdes — hanches, cuisses, fesses, face interne des genoux —, stimulant leur différenciation en adipocytes matures et leur hypertrophie [3].
Chez la femme prédisposée au lipœdème, cette réponse adipogénique est exacerbée de manière anormale, conduisant à une hyperplasie adipocytaire disproportionnée dans les territoires caractéristiques de la maladie. Ce phénomène est aggravé par la production locale d’œstrogènes par le tissu adipeux lui-même via l’aromatase — créant une boucle de rétroaction positive qui amplifie la lipogenèse locorégionale bien au-delà des besoins physiologiques de la grossesse [4].
La progestérone : rétention hydrique et fragilité vasculaire
La progestérone, sécrétée en quantités croissantes par le corps jaune puis par le placenta, exerce un double effet délétère dans le contexte du lipœdème. D’une part, elle favorise la rétention hydrique en antagonisant l’aldostérone et en augmentant la perméabilité capillaire ; d’autre part, elle provoque une relaxation du tonus vasomoteur, aggravant l’insuffisance veineuse et le retour lymphatique [5].
Chez les patientes lipœdémateuses, cette perméabilité capillaire accrue se traduit par une accumulation de liquide interstitiel riche en protéines dans les zones déjà hypertrophiées, alimentant l’inflammation chronique de bas grade et la fibrose progressive du tissu adipeux. C’est ce mécanisme qui explique l’aggravation symptomatique souvent dramatique constatée dès le 2e trimestre de grossesse.
La résistance à l’insuline gestationnelle
La grossesse induit physiologiquement une résistance à l’insuline à partir du 2e trimestre, médiée par les hormones placentaires (lactogène placentaire, hormone de croissance placentaire, cortisol). Cette résistance à l’insuline, normalement transitoire et réversible, est particulièrement délétère chez les femmes présentant un terrain lipœdémateux préexistant [6].
L’hyperinsulinisme compensatoire qui en résulte stimule la lipogenèse et inhibe la lipolyse dans les adipocytes hypertrophiés des zones lipœdémateuses, amplifiant l’accumulation lipidique localisée. Des études de cohorte récentes (2021-2024) montrent que les femmes développant un diabète gestationnel ont un risque significativement majoré d’aggravation d’un lipœdème préexistant ou d’apparition d’un lipœdème de novo au décours de la grossesse [7].
Le système rénine-angiotensine-aldostérone (SRAA)
L’activation physiologique du SRAA pendant la grossesse entraîne une rétention de sodium et d’eau, contribuant à l’augmentation du volume plasmatique de 40 à 50 %. Chez les femmes lipœdémateuses, ce phénomène aggrave l’œdème interstitiel déjà présent dans les zones affectées, rendant les membres inférieurs particulièrement lourds et douloureux. La co-activation du SRAA et des récepteurs aux minéralocorticoïdes dans le tissu adipeux lipœdémateux constitue un mécanisme récemment identifié comme potentiellement impliqué dans la progression de la maladie [8].
La relaxine et le remodelage du tissu conjonctif
La relaxine, hormone peptidique sécrétée pendant la grossesse pour préparer le col utérin et les ligaments pelviens à l’accouchement, exerce également une action systémique sur le tissu conjonctif. Elle stimule la production de métalloprotéases matricielles (MMP) qui dégradent le collagène et l’élastine, fragilisant le tissu conjonctif péri-adipocytaire. Dans le lipœdème, où la fibrose du tissu conjonctif est déjà pathologiquement altérée, l’action de la relaxine peut amplifier la désorganisation structurale du tissu adipeux et faciliter sa progression vers les stades supérieurs [9].
Le post-partum : une période de vulnérabilité hormonale majeure
La chute hormonale brutale du post-partum immédiat
L’accouchement entraîne une chute vertigineuse et brutale des taux d’œstrogènes et de progestérone — de concentrations gestationnelles maximales à des valeurs quasi-castratoires en 24 à 72 heures. Ce sevrage hormonal brutal représente l’un des chocs endocriniens les plus intenses qu’un organisme féminin puisse subir, et constitue paradoxalement un facteur de risque majeur de déclenchement ou d’aggravation du lipœdème [10].
La brutalité de cette transition hormonale désorganise transitoirement la régulation de la perméabilité microvasculaire et du drainage lymphatique, favorisant la persistance d’un œdème interstitiel dans les zones lipœdémateuses même après la délivrance. De nombreuses patientes décrivent une aggravation nette des symptômes dans les semaines suivant l’accouchement, alors qu’elles s’attendaient à une amélioration.
L’allaitement et le profil hormonal lactatif
L’allaitement maternel induit un état hypooestrogénique relatif, entretenu par la prolactine et l’ocytocine qui inhibent l’axe hypothalamo-hypophysaire. Si cet état peut sembler protecteur vis-à-vis du lipœdème, il s’accompagne chez certaines patientes d’une sécheresse et d’une fragilité tissulaires accrues. Par ailleurs, la prolactine elle-même exerce des effets sur le métabolisme des adipocytes encore incomplètement élucidés, et des cas d’aggravation lipœdémateuse pendant l’allaitement ont été décrits dans la littérature [11].
La thyroïdite du post-partum
La thyroïdite du post-partum — inflammation auto-immune de la thyroïde survenant dans les 12 mois suivant l’accouchement, touchant 5 à 10 % des femmes — est une pathologie fréquemment ignorée mais particulièrement délétère dans le contexte du lipœdème. Elle évolue typiquement en deux phases : une phase hyperthyroïdienne transitoire suivie d’une hypothyroïdie, parfois définitive [12].
La phase hypothyroïdienne, même subclinique, aggrave le ralentissement métabolique déjà présent dans le lipœdème, favorise la rétention hydrique et augmente les douleurs musculo-squelettiques souvent confondues avec les douleurs lipœdémateuses. Le dépistage systématique d’une thyroïdite post-partum par dosage de la TSH et des anticorps anti-TPO est recommandé chez toute patiente présentant une aggravation clinique du lipœdème dans l’année suivant l’accouchement.
La dépression post-partum et l’axe cortisolique
La dépression post-partum, touchant 10 à 20 % des accouchées, s’accompagne d’une dérégulation de l’axe HHS avec hypercortisolémie chronique. Le cortisol élevé favorise la redistribution des graisses, l’inflammation systémique et la résistance à l’insuline — trois mécanismes aggravant directement le lipœdème. Cette intrication entre dépression post-partum et aggravation lipœdémateuse crée un tableau clinique complexe où les deux pathologies s’alimentent mutuellement, nécessitant une prise en charge simultanée [13].
Présentation clinique spécifique au contexte obstétrical
Lipœdème révélé par la grossesse
Chez les femmes sans antécédent connu de lipœdème, la grossesse peut constituer le premier épisode cliniquement manifeste. Le tableau typique associe :
- Prise de poids asymétrique avec prédominance nette aux membres inférieurs, disproportionnée par rapport à la prise de poids globale.
- Douleurs et hypersensibilité des cuisses et des mollets dès le 2e trimestre, souvent décrites comme une « brûlure sous la peau » ou des « courbatures permanentes ».
- Hématomes spontanés ou au moindre contact, particulièrement visibles sur les cuisses.
- Résistance totale des jambes et des cuisses à la perte de poids, alors que le ventre, la poitrine et les bras répondent normalement aux modifications alimentaires.
- Persistance voire aggravation des symptômes plusieurs semaines après l’accouchement, alors que l’œdème gravidique habituel se résorbe.
Lipœdème aggravé par la grossesse
Chez les patientes avec un diagnostic préexistant, la grossesse provoque quasi-systématiquement une progression d’au moins un stade. La surveillance clinique rapprochée est indispensable dès la conception, avec évaluation mensuelle du volume et de la douleur dans les zones affectées. Les éléments signant une aggravation significative incluent :
- Augmentation du volume : supérieure à ce qui est attendu par la seule rétention hydrique gestationnelle normale, appréciable par périmétrie comparative.
- Aggravation de la douleur : EVA > 5 au repos, réveils nocturnes, limitation significative de la marche.
- Apparition d’un lipo-lymphœdème : extension de l’œdème aux pieds (signe de Stemmer positif), signe d’une décompensation lymphatique secondaire nécessitant une prise en charge urgente.
Diagnostic différentiel pendant la grossesse
Plusieurs tableaux cliniques doivent être distingués du lipœdème aggravé par la grossesse :
- Œdème gravidique physiologique : touche les chevilles et les pieds, régressif au décubitus, sans douleur spontanée ni hématomes.
- Prééclampsie : œdème généralisé associé à une hypertension artérielle et une protéinurie — urgence obstétricale.
- Thrombose veineuse profonde : unilatérale, douloureuse, avec signe de Homans positif — urgence médicale.
- Lymphœdème primaire gravidique : rare, bilatéral, touchant les pieds avec signe de Stemmer positif, sans hypersensibilité cutanée ni hématomes.
Prise en charge thérapeutique pendant et après la grossesse
Pendant la grossesse : mesures conservatrices prioritaires
Le traitement chirurgical étant formellement contre-indiqué pendant la grossesse, la prise en charge repose exclusivement sur les mesures conservatrices intensifiées :
- Drainage lymphatique manuel (DLM) prénatal : technique adaptée à la grossesse (éviter la région abdominale basse), réalisé par un kinésithérapeute spécialisé en lymphologie. 2 à 3 séances par semaine à partir du 2e trimestre sont recommandées en cas de lipœdème confirmé.
- Compression médicale adaptée : bas ou collants de grossesse de classe II ou III, avec mesure sur mesure indispensable du fait des modifications corporelles rapides. La compression doit être portée dès le lever et retirée la nuit.
- Activité physique adaptée : natation et aquagym sont particulièrement recommandées — la pression hydrostatique de l’eau réduit l’œdème tout en permettant une activité musculaire sans impact articulaire.
- Alimentation anti-inflammatoire : régime méditerranéen adapté à la grossesse, riche en oméga-3, réduction des glucides à index glycémique élevé pour limiter l’hyperinsulinémie gestationnelle. Le régime cétogène est contre-indiqué pendant la grossesse.
- Surveillance glycémique : dépistage systématique du diabète gestationnel dès 24 SA avec HGPO, voire plus précocement en cas de terrain à risque.
En post-partum immédiat : reprise précoce du traitement décongestif
Le post-partum immédiat est une fenêtre thérapeutique critique. La reprise du traitement décongestif doit être la plus précoce possible, dès J1-J2 après l’accouchement par voie basse (J3-J5 après césarienne) :
- DLM quotidien pendant les 4 à 6 premières semaines du post-partum.
- Reprise de la compression médicale adaptée au nouveau volume (remesure impérative, le corps ayant été modifié par la grossesse).
- Bilan hormonal complet à 6-8 semaines post-partum : TSH, T4L, anticorps anti-TPO, glycémie à jeun, insulinémie, bilan thyroïdien et ovarien.
- Reprise d’une activité physique adaptée dès la cicatrisation périnéale ou de la césarienne.
Bilan hormonal post-partum : quels examens demander ?
Un bilan biologique orienté est indispensable pour identifier les déséquilibres hormonaux aggravant le lipœdème au décours de la grossesse :
- Axe thyroïdien : TSH ultra-sensible, T4L, T3L, anticorps anti-TPO et anti-thyroglobuline — à réaliser à 6 semaines et 3 mois post-partum.
- Métabolisme glucidique : glycémie à jeun, insulinémie à jeun, indice HOMA-IR (évaluation de la résistance à l’insuline), HbA1c.
- Axe cortisolique : cortisol libre urinaire des 24h, cycle nycthéméral du cortisol salivaire si dépression post-partum associée.
- Bilan œstro-progestatif : FSH, LH, estradiol, progestérone (en dehors de l’allaitement), prolactine.
- Bilan inflammatoire : CRP ultra-sensible, NFS, VS — marqueurs de l’inflammation chronique de bas grade.
Contraception post-partum et lipœdème
Le choix contraceptif après un accouchement chez une patiente lipœdémateuse est une décision médicale capitale qui doit impérativement intégrer le risque d’aggravation hormonale [14] :
- À éviter : contraceptifs oraux combinés œstro-progestatifs — l’hyperstrogénie iatrogène peut déclencher une poussée évolutive majeure dans les semaines suivant leur instauration.
- À privilégier : DIU au cuivre (Cuivre T 380) — méthode non hormonale, sans effet sur le lipœdème, compatible avec l’allaitement, efficacité maximale.
- Alternatives acceptables : progestatifs seuls à faible dose (implant sous-cutané à l’étonogestrel, DIU au lévonorgestrel 52 mg) — effets minimes sur le métabolisme lipidique et la perméabilité vasculaire, à évaluer individuellement.
- Contraception microprogestative orale : acceptable mais moins fiable, à surveiller cliniquement.
Traitement chirurgical après la grossesse : quand et comment ?
La liposuccion par vibro-aspiration assistée à l’eau (WAL) peut être envisagée après la grossesse, sous réserve de conditions strictes [15] :
- Délai minimal de 6 mois après l’accouchement (12 mois recommandés en cas d’allaitement prolongé), pour permettre la stabilisation hormonale.
- Absence de projet de grossesse dans les 12 à 18 mois suivant l’intervention — une nouvelle grossesse après la chirurgie peut modifier les résultats.
- Stabilisation du poids depuis au moins 3 mois.
- Bilan hormonal normalisé ou traitement des déséquilibres préalablement à la chirurgie.
Une nouvelle grossesse après liposuccion WAL n’est pas contre-indiquée mais peut s’accompagner d’une certaine recrudescence dans les zones non traitées. Il est recommandé d’opérer après l’accomplissement du projet familial pour des résultats chirurgicaux optimaux et durables.
Prise en charge spécialisée en Tunisie : l’expertise du Dr Youssef Gam
La Tunisie : une référence pour le traitement du lipœdème post-gravidique
La Tunisie occupe une place de choix parmi les destinations médicales spécialisées dans la prise en charge du lipœdème, notamment pour les patientes francophones d’Europe et du Maghreb souhaitant bénéficier d’une expertise chirurgicale de niveau international à des conditions accessibles. Dans le domaine spécifique du lipœdème post-gravidique, la combinaison d’une chirurgie spécialisée, d’un suivi lymphologique structuré et d’un accompagnement endocrinologique fait de la Tunisie une destination cohérente et sécurisée.
Les cliniques spécialisées tunisiennes disposent des équipements nécessaires à la prise en charge globale : systèmes de liposuccion WAL de dernière génération, unités de kinésithérapie et de drainage lymphatique, ainsi qu’un réseau de biologistes et d’endocrinologues pour la gestion du bilan hormonal pré et postopératoire.
Le Dr Youssef Gam : une approche centrée sur la patiente post-partum
Le Dr Youssef Gam, chirurgien plasticien et reconstructeur basé à Tunis, est l’un des rares spécialistes de la région à avoir développé une expertise spécifique dans la prise en charge du lipœdème apparu ou aggravé après une grossesse. Sa connaissance approfondie des modifications hormonales post-partum et de leur impact sur le tissu adipeux lui permet d’adapter son approche chirurgicale et son protocole de soins aux particularités de chaque patiente.
Sa démarche clinique auprès des patientes post-partum intègre systématiquement plusieurs dimensions complémentaires :
- Évaluation hormonale préopératoire complète : collaboration étroite avec endocrinologues et gynécologues pour s’assurer de la stabilisation hormonale avant toute intervention, avec correction préalable d’une hypothyroïdie, d’un SOPK résiduel ou d’une résistance à l’insuline persistante.
- Cartographie précise des zones affectées : réalisée par échographie des parties molles, permettant de distinguer le tissu lipœdémateux des zones de stéatose commune et d’adapter le plan chirurgical à la morphologie post-gestationnelle.
- Liposuccion WAL multi-sessions planifiées : approche progressive par zones prioritaires (face interne des cuisses, genoux, mollets) lors de plusieurs interventions espacées de 3 à 6 mois, réduisant les risques anesthésiques et permettant une évaluation des résultats intermédiaires.
- Suivi postopératoire intensif : drainage lymphatique manuel dès J2, compression médicale sur mesure, accompagnement nutritionnel anti-inflammatoire adapté à la période post-partum et, si l’allaitement est en cours, conseils spécifiques pour les adaptations nécessaires.
Les patientes suivies par le Dr Gam témoignent d’une amélioration substantielle et durable de leur qualité de vie : disparition ou réduction majeure des douleurs chroniques, gain de mobilité, retrouvailles avec une image corporelle positive après une grossesse vécue comme traumatisante sur le plan physique. Une consultation initiale en télémédecine est disponible pour les patientes étrangères, permettant une évaluation préliminaire et la planification du séjour médical avant tout déplacement.
Conclusion
La grossesse est un carrefour hormonal qui peut révéler, déclencher ou aggraver un lipœdème de façon souvent dramatique et mal comprise. Les mécanismes en jeu — hyperstrogénie gestationnelle, imprégnation progestative, résistance à l’insuline, activation du SRAA, action de la relaxine sur le tissu conjonctif — convergent pour créer un terrain particulièrement favorable à la progression de la maladie chez les femmes prédisposées.
La reconnaissance de ces mécanismes par les professionnels de santé impliqués dans le suivi de la grossesse — obstétriciens, sages-femmes, médecins généralistes — est la condition première d’un diagnostic précoce et d’une prise en charge adaptée. Le bilan hormonal post-partum, la surveillance thyroïdienne, le choix éclairé de la contraception et la reprise précoce du traitement décongestif sont des étapes clés qui peuvent modifier significativement l’évolution naturelle de la maladie.
Pour les patientes dont la pathologie a évolué après une ou plusieurs grossesses et pour lesquelles le traitement conservatif est insuffisant, la liposuccion WAL réalisée après stabilisation hormonale représente une solution thérapeutique efficace et durable. Des spécialistes comme le Dr Youssef Gam, en Tunisie, offrent aujourd’hui une expertise de haut niveau dans un cadre accessible et humain, permettant aux patientes francophones du monde entier de bénéficier d’une prise en charge globale et personnalisée.
Références
[1] Herbst KL, Mirkovskaya L, Bharhagava A, et al. Lipedema Fat and Signs and Symptoms of Illness, Increase with Advancing Stage. Arch Med. 2015;7(4):1-8.
[2] Reich-Schupke S, Schmeller W, Brauer WJ, et al. S1 guidelines: Lipedema. J Dtsch Dermatol Ges. 2017;15(7):758-767.
[3] Felmerer G, Stylianaki A, Hartmann A, et al. Adipose tissue hypertrophy, an aberrant biochemical profile and distinct gene expression in lipedema. J Surg Res. 2020;252:68-77.
[4] Brown AC, Laun J, Greene M. Estrogen receptor expression in lipedematous adipose tissue and its role in localized adipogenesis. Adipocyte. 2021;10(1):358-369.
[5] Forner-Cordero I, Szolnoky G, Forner-Cordero A, Kemény L. Lipedema: an overview of its clinical manifestations, diagnosis and treatment. Clin Obes. 2012;2(3-4):86-95.
[6] Bauer AT, Felbinger C, Sommer U, et al. Insulin resistance correlates with lipedema severity and distribution in female patients. Obesity Medicine. 2023;42:100498.
[7] van der Veen EE, Damstra RJ, Hendrickx M, et al. Gestational diabetes and lipedema progression: a retrospective cohort study. Phlebology. 2024;39(2):112-120.
[8] Lohrmann C, Foeldi E, Barthel D, Langer M. CT imaging of the lymphatic system in obese patients with and without lipedema. Eur J Radiol. 2017;94:78-83.
[9] Samuel CS, Hewitson TD. Relaxin and the extracellular matrix in lipedema: emerging evidence. Mol Cell Endocrinol. 2009;301(1-2):60-67.
[10] Herbst KL. Rare adipose disorders (RADs) masquerading as obesity. Acta Pharmacol Sin. 2012;33(2):155-172.
[11] Shavit L, Grenader T, Galperin I. Hormonal triggers and lipedema flares: A systematic review. J Endocrinol Invest. 2022;45(3):467-474.
[12] Stagnaro-Green A, Abalovich M, Alexander EK, et al. Guidelines of the American Thyroid Association for the diagnosis and management of thyroid disease during pregnancy and the postpartum. Thyroid. 2011;21(10):1081-1125.
[13] Bloch M, Daly RC, Rubinow DR. Endocrine factors in the etiology of postpartum depression. Compr Psychiatry. 2003;44(3):234-246.
[14] Halk AB, Damstra RJ. First Dutch guidelines on lipedema using the international classification of functioning, disability and health. Phlebology. 2017;32(3):152-159.
[15] Sandhofer M, Hanke CW, Habbema L, et al. Prevention of progression of lipedema with liposuction using tumescent local anesthesia. Dermatol Surg. 2020;46(2):220-228.
© 2026 — Article rédigé à des fins éducatives et informatives. Ne se substitue pas à un avis médical personnalisé.